Kas yra alifatiniai angliavandeniliai?
Alifatiniai angliavandeniliai yra organiniai junginiai, kurių molekulėse yra tik viena jungtis. Tai apima alkanus ir cikloparafinus, jų savybės bus laikomos mūsų medžiagoje.

Bendra alkanų formulė
Šios klasės atstovai būdingipagal bendrąją formulę CnH2n + 2. Parafinai apima visus junginius, turinčius atvirą grandinę, kur atomai sujungiami paprastais ryšiais. Dėl to, kad normaliomis sąlygomis alifatiniai angliavandeniliai yra mažai aktyvūs junginiai, jie gavo savo pavadinimą "parafinai". Išsiaiškinsime kai kurias šios klasės atstovų struktūros ypatybes, obligacijų molekulėse pobūdį, taikymo sritį.

Trumpas metano aprašymas
Kaip paprasčiausias šios klasės atstovas, mes galime paminėti metano. Tai tas, kuris pradeda alifatinę angliavandenilių grupę. Mes atskleidžiame savo išskirtines savybes.
Metanas yra normaliomis sąlygomisdujinė medžiaga bekvapė ir bespalvė. Šis junginys yra natūraliai suformuotas skaldant be gyvų gyvūnų ir augalų organizmų deguonies. Pavyzdžiui, jis randamas gamtinėse dujose, todėl šiuo metu jis yra naudojamas dideliais kiekiais kaip degalai gamyboje ir kasdieniame gyvenime.
Kokią cheminę jungtį turi šie angliavandeniliai? Alifatiniai, ribojantys organiniai junginiai yra kovalentinės poliarinės molekulės.
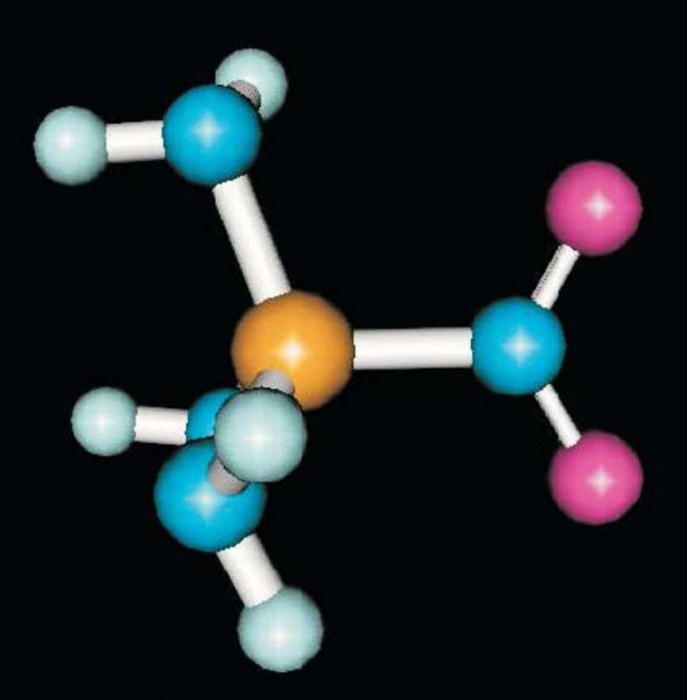
Metano molekulė yra tetraedrinė formamolekulė, joje yra anglies atomų hibridizacija sp3, kuri atitinka valentingumo kampą 109 ° 28 minučių. Būtent dėl šios priežasties alifatiniai angliavandeniliai yra chemiškai mažai aktyvūs junginiai.

Metano homologų savybės
Be metano gamtinėse dujose ir aliejuje,Kiti angliavandeniliai, kurių struktūra yra panaši. Pirmieji keturi homofobinių parafinų serijų atstovai yra dujinių agregatų būklėje, turi nedidelį tirpumą vandenyje.
Kaip giminaitisCdHy virimo ir lydymosi taškų padidėjimas molekulinėje masėje. Tarp atskirų serijos atstovų yra tam tikras skirtumas CH2, kuris vadinamas homologiniu skirtumu. Tai tiesioginis teiginys, kad junginys priklauso šiai ekologinei serijai.
Visi alifatiniai angliavandeniai yra medžiagos, kurios lengvai tirpsta organiniuose tirpikliuose.

Serijos izomerizmas
Reikšminga daugybei parafinų atstovųanglies skeleto izomerizmas. Tai paaiškinama dėl anglies atomo aplinkinių cheminių jungčių erdvinio sukimosi galimybių. Pavyzdžiui, norint sujungti C4H10 kompoziciją, galite pasiimti angliavandenilį su tiesia anglies skeletele - butanu. Kadangi struktūrinis izomeras bus 2-metilpropanas, turintis šakotą struktūrą.
Tarp tipiškų cheminių savybių yra būdingaparafinams, būtina atkreipti dėmesį į pakaitines reakcijas. Ryšių prisotinimas paaiškina reakcijos sudėtingumą, jos radikalų mechanizmą. Norint gauti halogenintų alifatinių angliavandenilių darinių, būtina atlikti halogeninimo reakciją esant UV spinduliavimui. Šios sąveikos grandinės pobūdis pastebimas visuose šios serijos atstovuose. Gauti produktai vadinami halogeno dariniais. Jie plačiai naudojami chemijos pramonėje kaip organiniai tirpikliai.
Be to, visi alifatiniai ir aromatiniaiangliavandeniliai dega deguonimi, susidaro vanduo ir anglies dioksidas. Priklausomai nuo anglies molekulės procentinio kiekio, išleidžiamas kitas šilumos kiekis. Nepriklausomai nuo priklausymo organinių junginių klasei, visi degimo procesai yra egzoterminės reakcijos, naudojamos kasdieniame gyvenime ir pramonėje.
Metano dehidrogenizavimas (vandenilio skaidymas) taip pat yra praktiškai pritaikytas. Dėl šio proceso susidaro acetienas, kuris yra vertinga cheminė žaliava.

Alkanų ir chlorintų alkanų naudojimas
Dichlormetanas, chloroformas, tetrachloretanas, skysčiai,kurie yra puikūs organiniai tirpikliai. Chloroformas ir jodoformas yra naudojami šiuolaikinėje medicinoje. Metano skilimas yra vienas iš pramoninių metodų sodriems produktams gaminti, kuris yra būtinas rašaliniams dažams gaminti. Metanas laikomas pagrindiniu dujinio vandenilio gamybos šaltiniu chemijos pramonėje, kuris vyksta amoniako gamybai, taip pat daugelio organinių medžiagų sintezei.
Nesotieji angliavandeniliai
Nesotieji alifatiniai angliavandeniliai yradaugelio etileno ir acetileno atstovai. Leiskite mums išanalizuoti jų pagrindines savybes ir programas. Alkenuose būdingas dvigubas ryšys, todėl bendra serijos formulė yra tokia: CnH2n.
Atsižvelgiant į nesočiųjų šių medžiagų pobūdį,galima pastebėti, kad jie jungiasi į reakciją: hidrinimas, halogeninimas, hidratacija, halogeninimas. Be to, daugelio etileno atstovai gali polimerizuoti. Būtent ši ypatybė, dėl kurios šios klasės atstovai reikalauja šiuolaikinės chemijos gamybos. Polietilenas ir polipropilenas yra medžiagos, kurios sudaro pagrindą polimerų pramonei.
Acetilenas yra pirmasis serijos turėtojasBendra formulė yra CnH2n-2. Tarp šių junginių būdingų savybių galima išskirti trijų ryšių buvimą. Jo buvimas paaiškina junginio reakciją su halogenais, vandeniu, vandenilio halogenidu, vandeniliu. Jei trivietis junginys tokiuose junginiuose yra pirmoje pozicijoje, tada alkilinams būdinga kokybinė pakaitalo reakcija su kompleksine sidabro druska. Būtent šis gebėjimas yra kokybinė reakcija į alkiną, naudojamą jo aptikimui mišinyje su alkenu ir alkanais.
Aromatiniai angliavandeniai yra cikliniai nesotieji junginiai, todėl jie nelaikomi alifatiniais junginiais.
Išvada
Nepaisant kiekybinės sudėties skirtumo,egzistuoja ribinių ir nesočiųjų alifatinių junginių atstovai, jie yra panašūs kokybe, molekulėse yra anglies ir vandenilio. Kiekybinės sudėties (įvairios bendrosios formulės) skirtumai sočiųjų ir nesočiųjų CCl2 atstovuose paaiškina įvairių produktų gavimo reakcijų mechanizmų skirtumus.
Štai kodėl atstovai iš visų klasių tokiųjunginiai patenka į degimo reakcijas, susidaro anglies dioksidas, vanduo, atpalaiduojantis tam tikrą šiluminę energiją, dėl ko reikalingas degalų naudojimas kasdieniame gyvenime ir pramonėje.
</ p>


